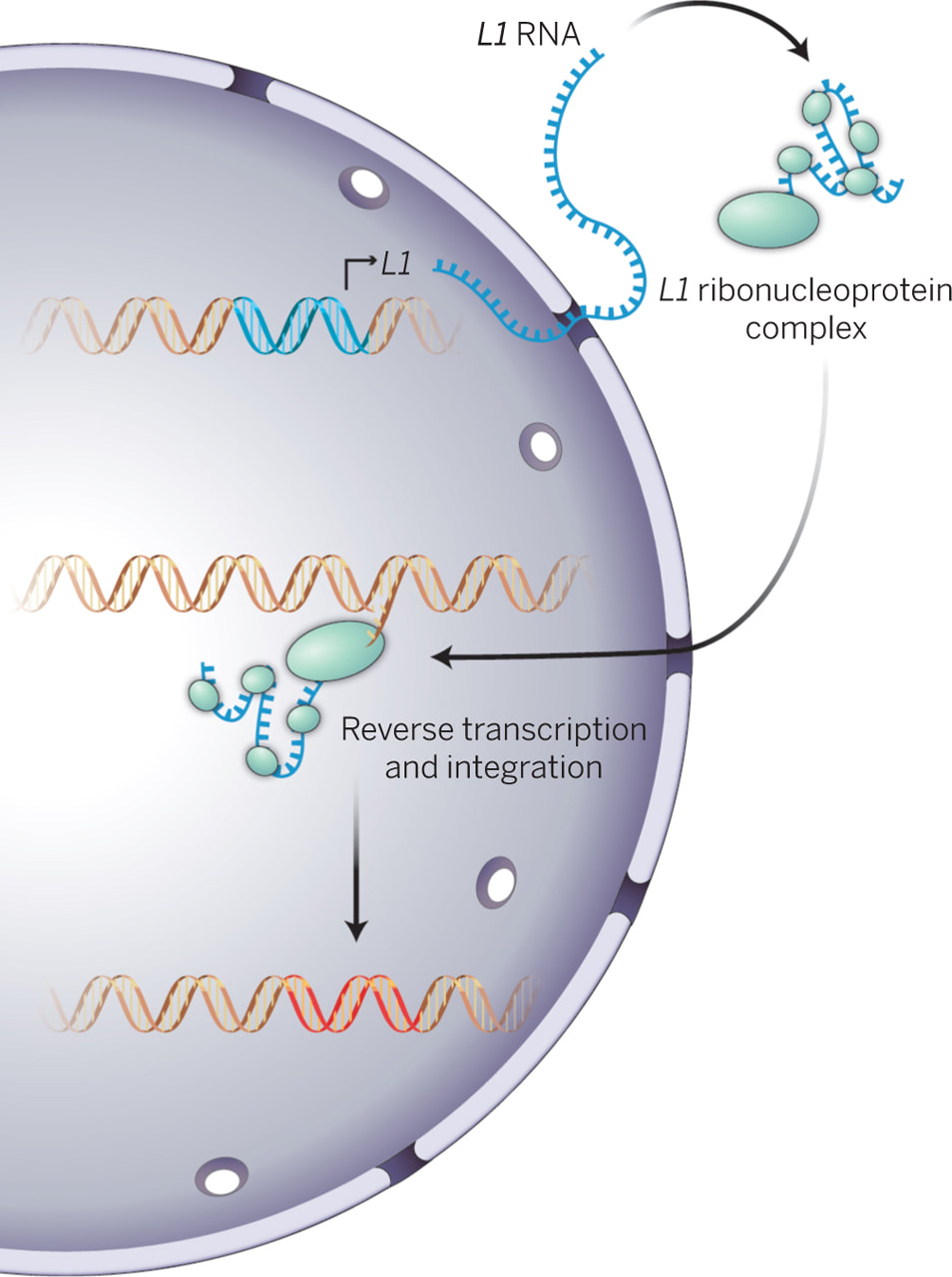
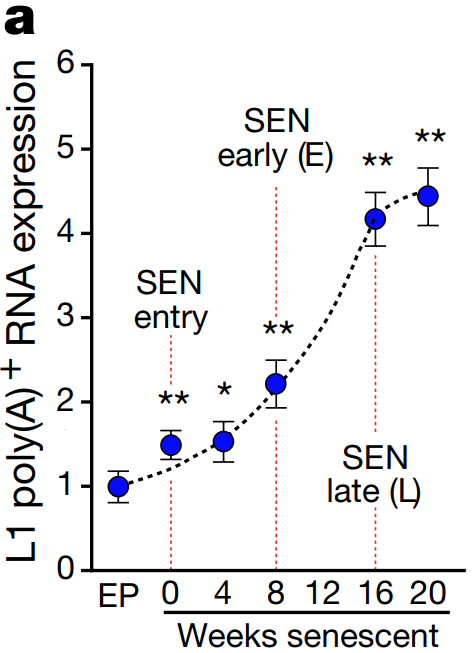
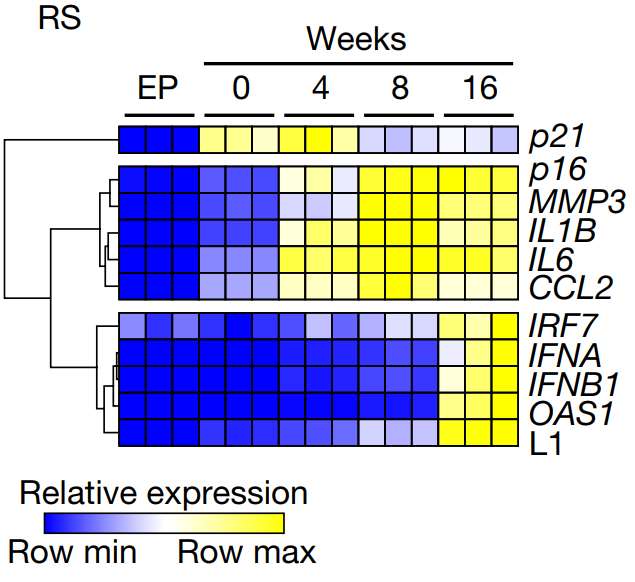
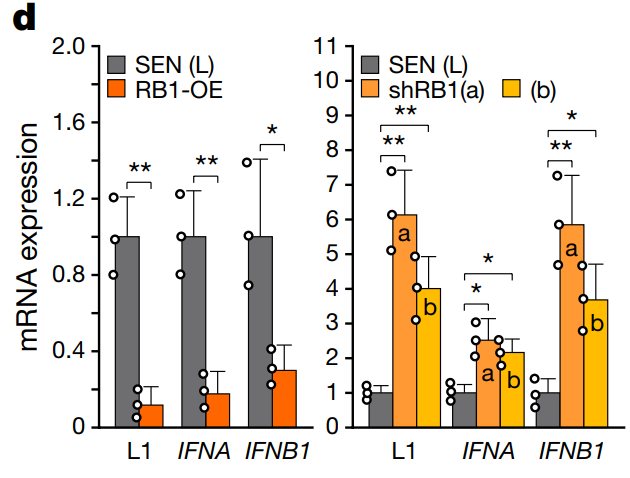
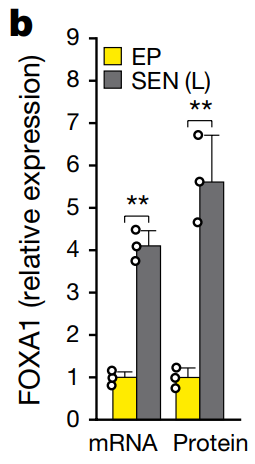
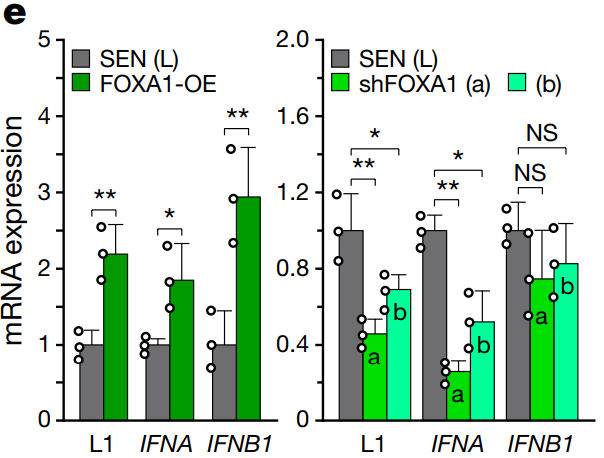
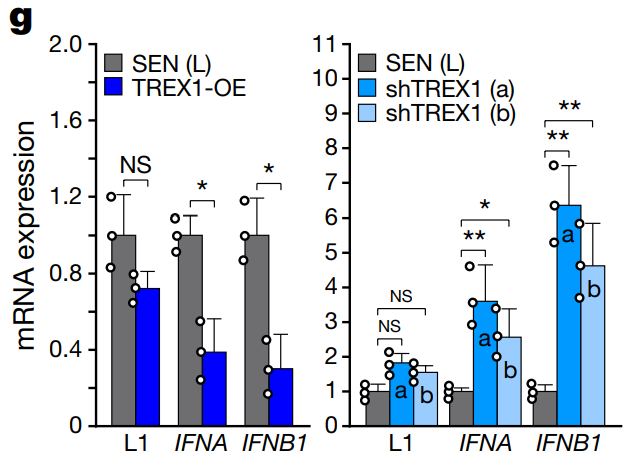
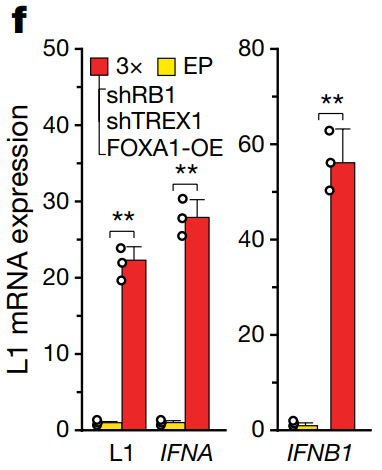
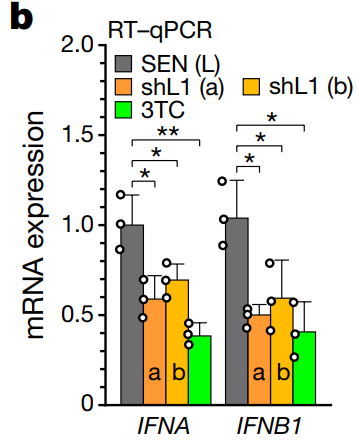
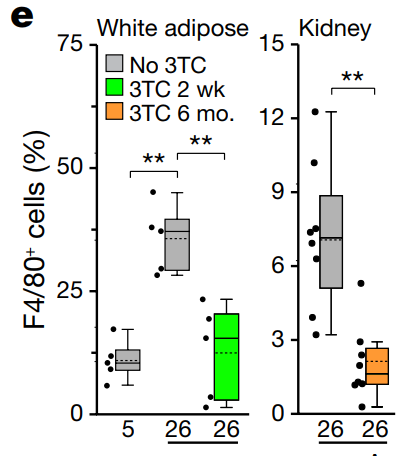
노화 세포의 트렌스포존이 노화-염증을 일으킨다L1 drives IFN in senescent cells and promotes age-associated inflammation De Cecco et al. 2019 Inhibition of 'jumping genes' promotes healthy ageing Childs & van Deursen 2019 Sleeping dogs of the genome Gorbunova et al. 2014 지난번 DNA 속 시한폭탄이란 글에서 생물의 유전자 속에 숨어 있는 LINE-1 이라는 트랜스포존이 노화의 한 원인이라 설명한 바 있다. 당시 경쟁 연구팀의 논문이 먼저 나온 것에 굉장히 착잡해 했는데 다행히 포닥 형의 논문도 지난달 발표 됐다. 3년 동안 끈질긴 리뷰어와 싸우면서 받은 스트레스가 한 번에 날아간 듯 보인다. 조금 늦었지만, 내게 너무도 친숙한, 정말 오래 숙성된 이 논문을 소개하도록 하겠다. 먼저 지금의 노화 연구가 어떻게 시작됐는지 간략하게 설명하겠다. 1961년 레오나르드 헤이플릭 박사가 발표한 논문이 모든 것의 발단이다 (출처). 당시 백신 연구를 하고 있던 헤이플릭 박사는 실험에 필요한 세포를 배양하던 중 한 가지 특이점을 발견하였는데 아주 오랜 시간 배양한 세포들은 건강해 보이지만 분열을 하지 않는다는 것이다. 그 당시까지만 해도 세포들은 양분만 잘 공급해 주면 무한정 증식한다 알고 있었다. 특히 그 유명한 불로불사 HeLa 세포가 막 등장한 시기라서 모든 세포가 무한히 증식한다 생각하기 쉬울 때였다. 돌이켜 보면 HeLa는 정말 우연히도 완벽한 불멸화가 된 세포였고 마침 세포 연구가 활발히 시작되던 시기에 나타나 전 세계 과학자들에게 널리 배포되었던 건데.. 헤이플릭 박사가 특별히 더 성실했던 건지 아니면 실험을 게을리 했던 건지 모르겠지만 헤이플릭 박사가 배아 섬유아 세포를 약 일 년간 배양하자 더 분열을 하지 않는 상태가 되었다. 일 년 동안 실험을 안 하고 배양기에 세포를 방치한 것인지 열심히 실험하면서 일부는 따로 때어 놓은 건지는 본인만 알 것이다. 어쨌든 이렇게 밝혀진 게 그 유명한 헤이플릭 한계로 세포가 일정 횟수의 분열을 하고 나면 더 분열을 하지 못하는 상태에 이른다. 이후 살아 있으나 더 분열하지 못하는 세포들을 세포 노화 상태, 혹은 세네센스 (senescence) 상태라 부르게 됐다. 헤이플릭 한계가 발견된 지 약 10년 후엔 DNA가 분열할 때마다 조금씩 줄어들어 어느 정도 분열하면 더 분열이 불가능한 크리티컬 시점이 온다는 주장이 나왔고 이를 실험적으로 입증한 공로로 엘리자베스 블랙번 박사와 몇몇이 노벨상을 수상받기도 하였다. 흔히 알고 있는 텔로미어로 인한 노화 이론이 블랙번 박사의 연구에서 나온것이고 노벨상과 함께 언론을 타게 돼서 인지도가 높다. 백발이 되셨지만 이분은 지금도 열심히 텔로미어를 파고 계시고 종종 컨퍼런스에 오셔서 발표도 하신다. 근래에 와서 노화 연구는 아주 세분화 되고 다양해졌다. 후성유전학, 면역학, 오토파지, 사이토킨 등 여러 방면에서 중대한 발견들이 있었고 앞으로 짬짬이 설명할 기회가 있길 바란다. 우리 실험실은 본래 암을 연구하다 세네센스 (노화 세포) 연구로 넘어온 케이스다 (출처). 암과 노화는 굉장히 밀접한 관계가 있어 암으로 시작해 노화로 넘어온 연구팀이 많이 있다. (내 학부 연구는 아예 대놓고 암 관련 프로젝트와 세포 노화 관련 프로젝트를 병행하였다). 듣기로는 수년 전 실험실에 있던 한 대학원생이 이미 세네센스에 도달한 세포들을 몇 달간 방치시켰던 게 이번 논문의 시발점이었다 한다. 생물학은 굉장히 빠른 페이스로 움직이기 때문에 어쩔 수 없이 오랜 시간 기다려 봐야 하는 노화 연구를 하는 사람들은 항상 초조할 수밖에 없다. 세네센스 상태를 만들기 위해 거의 1년 동안 기다려야 하므로 더 분열을 안 한다 확인이 되면 바로 실험을 시작해 몇주 안에 노화 세포를 다 소진한다. 그런데 어떤 배짱이 심보의 박사 학생이 세네센스 세포들을 잔뜩 만들어 놓고도 실험을 차일피일 미루다 몇 달을 더 배양하게 되었다. 마치 헤이플릭 박사가 백신 실험을 위해 기르던 세포를 너무 오래 둬서 헤이플릭 한계를 발견한 거 같이, 한 대학원생이 방치한 포스트 헤이플릭 한계의 세포가 또 다른 단계에 들어선 것이다. 이런 걸 보면 노화 연구는 그냥 마음을 비우고 새로운 특이점이 나올 때까지 무작정 기다려 보는 것도 하나의 전략인 거 같다. 어쨌든 우리 실험실은 새로운 단계의 노화 세포를 딮 세네센스 (deep-senescence)라고 칭하고 딮 세네센스에 도달한 세포들이 어떤 식으로 노화를 주도하는지 연구하였다. 이전부터 세네센스로 비롯된 트랜스포존을 연구하던 중이었기 때문에 딮 세네센스에서 나타나는 트랜스포존 활동과 조직 노화로의 연결 고리 입증에 초점을 두었다. 트랜스포존에 대해선 이전 글 (DNA 속 시한폭탄) 에서 짧게 설명하였으나 링크 타고 넘어가는 귀찮음을 알기 때문에 다시 설명해 보겠다. 우리가 주목해야 할 것은 레트로트렌스포존이란 것들인데 (retrotransposable elements) DNA 속에 잠재되어 있다가 RNA로 전사되고 다시 DNA로 역전사하면서 새로운 유전자에 침투한다. 어디서 많이 본 그림 아닌가? RNA 베이스의 바이러스들이 이런 식으로 증식한다. 대표적으로 HIV 가 있다. 우리 유전자 속 대부분 레트로트렌스포존은 비활성화되어 있는데 아직도 움직이는 몇 개가 있고 그게 LINE-1 이라 불리는 애들이다. LINE-1 은 아마 아주 오래전 인간을 감염한 바이러스로 추정되며 오랜 시간 인간의 몸은 이 바이러스를 잡아내기 위해 싸워왔다. 바이러스가 날뛴다면 순식간에 수천, 수만 개로 복제되 유전자 곳곳에 들어가게 될 것이고 인간의 유전자는 엉망진창이 될 것이다. 이를 막기 위해 감염된 바이러스를 제거하지 못할 망장 더 늘어나지 않게 하기 위해 바이러스가 들어간 유전자를 통째로 비활성화시켜 전사의 가능성을 제거하였다. 그런데도 방어막을 뚫고 하나둘씩 늘어난 바이러스 때문에 이미 인간의 DNA 중 무러 66% 가 LINE-1 바이러스 서열이 되어 버렸다. 지금도 조금씩 바이러스의 지분은 늘어나는 중이고 말이다 (신생아 100~300명 중 한명 꼴로 LINE-1 이 하나 더 추가된다). 초기 LINE-1 연구는 생식세포로 국한되었다. 아무래도 유전자 문제는 다음 세대로 넘겨지냐 마냐가 가장 중요하니까 그 외 세포에서 일어나는 일에는 관심이 없었다. 그런데 LINE-1 이 단순히 새로운 유전질환을 만들 가능성만 있는 게 아니다. 우리 몸은 자녀 생산을 하는 순간까진 꽤 효과적으로 LINE-1 의 활동을 저지한다 (인간 DNA의 66% 가 LINE-1 인걸 고려하면 100 명 중 한명마다 LINE-1 이 하나 세어나가는 것도 대단한 선방이다. 인구 수를 생각하면 LINE-1 의 증가 속도가 위협적이지 않다 말할 순 없지만..). 그런데 자녀 생산이 끝나고 나이가 들면 LINE-1 방어 체계가 하나씩 무너지기 시작하고 LINE-1 이 날뛰며 세포가 급속도로 망가지게 된다. 몸이 노쇠해지는 것이다. 연구팀이 제시하는 노화 이론은 이렇다: 젊었을 땐 세포들이 LINE-1 을 잘 억제하여 정상적인 유전자를 유지하고 이상적인 기능을 보존한다. 나이가 들면서 생겨난 노화 (세네센스) 세포는 LINE-1 감시 체계가 약화한 상태로 LINE-1 이 마구 날뛰기 시작한다. 게놈이 불안정해지고 세포가 염증 반응을 일으키며 조직의 기능이 떨어진다. 이러한 일이 몸의 곳곳에서 동시다발적으로 일어나는 걸 우리는 노화로 인지한다. 노화의 원인이 세네센스가 나타내는 LINE-1 활동이라면 이를 저지할 경우 노화를 저지할 수 있게 되는 것이다. 다행히도 인류는 LINE-1 과 같은 레트로바이러스에 대한 대처법을 이미 많이 연구해 뒀다. 몇몇 HIV 대항 약품이 LINE-1 에게도 상당히 효과적이고 HIV 약품으로 LINE-1 을 억제할 경우 노화 증상이 크게 줄어든다. 그럼 이제 데이터를 보며 위 사실들을 확인해 보겠다. 먼저 세네센스와 LINE-1 의 관계를 보여주는 그래프다. EP는 early passage의 약자로 아직 노화 세포 단계에 들어서지 않은 젊은 세포들의 수치다. 이를 1로 볼 때 노화 세포가 상대적으로 얼마나 많은 LINE-1 RNA를 보이는지 관찰했다. 세네센스에 도달한 직후인 SEN entry에 이미 유의미한 증가가 관찰되었고 세네센스에 들어선 후 8주가 지난 후에 거의 두배의 LINE-1 RNA가 발견되었다. 놀라운 건 노화 세포를 계속 방치했을 때다. 여기서 late senescence라 표기했으나 최근 deep-senescence란 용어를 밀고 있는 거 같은데 노화 세포를 16주 방치할 경우 무려 4배의 LINE-1 RNA가 발견된다. 더 중요한 건 이거다. 세네센스로 인한 노화 이론이 학계에서 바로 정설로 받아들여지지 못한 이유 중 하나가 노화의 원인으로 꼽히는 핵심 물질들을 세네센스에서 발견하지 못하였기 때문이다. 요즘 가장 핫한 건 인터페론 (IFN) 이라는 신호 물질인데 노인들을 보면 이 물질이 굉장히 많이 발견되고 아픈 것도 아닌데 온몸에 만성 염증이 나타난다. 위 표를 읽는 방법은 이렇다. 젊은 세포는 EP로 표기하였고 이후 세네센스에 들어선 지 각각 0, 4, 8, 16주가 지난 세포에서 얻은 결과다. 세로로는 검사해본 다양한 물질들이 나열되어 있고 노란색일수록 더 많이 검출됐다는 뜻이다. 보시다시피 p16, MPP3, IL6 등 흔히 세네센스와 연관되는 물질들은 다 세네센스 직후 나타나는 물질들이었다. 논란이 되었던 IFN 의 경우 8주 차까지도 검출되지 않다가 16주가 돼서야 대량 검출되었다. 다시 말해 지금까지 실험들은 너무 젊은 노화 세포로 해와서 올바른 결과를 보지 못한 것이다. 우리 몸이 노화 세포와 함께 수십 년을 사는 걸 생각해 보면 앞으로의 실험은 딮 세네센스 세포로 해야 하는 게 맞다. 그럼 왜 세네센스 세포들이 LINE-1 과 다른 핵심 노화 물질을 나타내는 것일까? 세네센스 세포들을 정밀 검사한 결과 연관성 있는 신호들을 몇 구별해 냈고 그중 3가지를 집중적으로 조명하였다. 첫 번째는 RB1이다. Retinoblastoma protein의 약자로 암 억제 단백질로 널리 알려져 있다. RB1은 불필요한 유전자의 발현을 막는다. 전사되지 말아야 할 유전자에 붙어 부호화시킨다. 추측건데 LINE-1 을 저지하는 첫 번째 방어막이 RB1 이 형성한 이질염색질 (heterochromatin) 일 것이다. 실험적 증거는 다음과 같다. 먼저 일반 세포의 RB1 발현량을 1이라 볼 때 세네센스에선 0.3 도 되지 않는다. 특히 딮 세네센스의 경우 거의 검출이 되지 않았다. 이는 젊은 세포가 유지하였던 이질염색질이 세네센스 세포에선 모두 풀어져 더 이상 선택적 유전자 억제가 되질 않는다 볼 수 있다. 보다 확실한 입증을 위해 이번엔 세네센스 세포에 RB1 발현을 강요해 봤다. RB1 수치를 높이는 것만으로 세네센스 세포의 LINE-1 과 IFN 수치가 대폭 줄어들었다 (왼쪽 그래프). 반대로 세네센스 세포의 RB1을 아예 제거할 경우 LINE-1 과 IFN1 수치가 더 높아짐이 관찰되었다. 두 번째 특이점은 비정상적으로 높은 FOXA1의 발현이었다. FOXA1이 왜 증가한 지는 확실치 않으나 증가한 FOXA1이 LINE-1의 프로모터에 붙으면서 LINE-1 전사를 유도하는 것으로 생각된다. 이전과 마찬가지로 FOXA1을 증폭시키거나 제거한 후 결과를 봤더니 FOXA1이 증폭될 경우 LINE-1 RNA 수치도 올라가고 FOXA1을 제거할 경우 LINE-1 수치가 내려갔다. 이는 FOXA1이 LINE-1 전사를 유도한다는 간접적인 증거다. 마지막으로 볼 것은 TREX1 이라는 DNA 제거 효소다. 어찌어찌하여 LINE-1 이 전사되고 DNA로 역전사될 경우 마지막 방어 수단으로 떠돌아다니는 DNA를 즉각 제거하여 증식을 멈출 수 있다. 예상할 수 있듯이 TREX1이 증폭될 경우 LINE-1 수치는 떨어지고 TREX1 이 줄어들 경우 LINE-1 수치가 올라간다. 노화 세포의 경우 3가지 방어 체계가 다 무너져 있다. 젊은 세포의 방어 체계를 똑같이 무너트리면 어떻게 될까? 결과는 놀라웠다. LINE-1 수치가 무려 20배 넘게 증가하고 IFNB1의 경우 거의 60배 증가하였다. 그런데 이것만으로 LINE-1의 증가가 노화 현상의 직접적인 원인이라 보긴 힘들지 않은가? 우연히 세네센스 세포의 LINE-1도 증가하고 다른 핵심 노화 물질도 증가한 거 아닌가? 보다 직접적인 증거를 위해 LINE-1을 억제한 후 어떤 변화가 나타나는지 지켜보기로 했다. 여러 방법이 사용됐지만 편의를 위해 3TC라는 HIV 대항 약품을 사용한 결과만 논하겠다. 3TC는 역전사 효소를 억제하는 약품으로 LINE-1 RNA가 DNA로 번역되는 걸 막아준다. 한 달간 세네센스 세포에 3TC를 준 경우 노화 핵심 물질인 IFN이 반 이상 줄어들었다. IFN이 노화의 대표적인 특징인 만성 염증을 일으키는 것을 생각해 볼 때 IFN의 하락은 염증 완화와 전체적인 기능 회복을 가져올 것으로 기대된다. 일단 논문에 실린 동물 실험 데이터는 3TC 투여 후 확연히 줄어든 면역 반응 (면역세포 갯수 저하) 밖에 없다. 보충 데이터에 뭐가 더 있을 수도 있지만 워낙 방대한 양이라 들여다보고 싶지 않다 (막상 보면 이것저것 또 설명해 주고 싶어질 거 같다..). 어쨌든 지방 세포에서 발견되는 면역세포의 양이 생후 5개월 때는 15% 미만이다가 26개월엔 30~40%를 육박하는데 3TC를 2주만 먹여도 거의 정상화 된다. 신장에서도 그만큼 확연하진 않으나 유의미한 변화가 나타났다. 3TC를 먹인 늙은 쥐의 신체 활동 역량을 확인하고자 미니 체육대회를 개최할 계획이었는데 실험이 자꾸 밀려서 그냥 협력 연구팀에 과제를 넘겨줘야 할지 모르겠다.
11 Comments
황서연
5/14/2019 04:50:01 am
너무 궁금한데 혹시 언제 게시될까요??
Reply
관리자
5/14/2019 05:51:44 am
한번 미루기 시작하니까 끝이 없네요.. 안그래도 다시 열심히 포스팅을 해야겠다 생각하고 있었습니다. 이번주 중에 써보도록 할께요.. 늦어도 이달 말에는 다시 포스팅 시작할거에요
Reply
JGH
8/6/2019 09:29:20 pm
이번에 대학원을 입학하면서 senescence 쪽을 공부하게 되었는데, 어지간한 리뷰논문보다 잘정리되어 있어서 초반에 개념잡는데 많이 도움이 되었습니다. 감사합니다.
Reply
관리자
8/7/2019 06:03:26 am
동지가 하나 늘었군요. 잘 해봅시다
Reply
JGH
8/7/2019 08:21:31 am
감사합니다. 많이 배우겠습니다. 저는 미토콘트리아쪽으로 접근하고 있습니다. MRPs 쪽으로..!
LEE
11/29/2019 04:16:03 am
약학대학에서 공부하고 있는학생입니다.. 세포노화 분야에대해서 많은 관심을 가지고있고 올려주신 내용 잘 읽고 있습니다
Reply
관리자
1/21/2021 09:06:11 am
댓글을 이제야 발견했네요.. 아직도 유효한 질문인지 모르겠지만 일단 연구 관심사를 조금 더 좁혀주셔야 할거 같습니다. 적당히 인지도 있는 대학 순으로 지원해서 합격하는 가장 좋은 곳을 가도 되지만 특별한 연구 주제가 잡혀있다면 그 연구의 최고 권위자 랩에 도전해 보실 수 있어요. 문제는 그 교수님이 속한 대학에 합격한다고 그 교수님과 함께 연구하는게 보장되는건 아닙니다. 랩에 자리가 없을 수도 있고 그냥 교수님이 안 뽑으실 수 있어요. 그래서 일반적으로 함께 연구하기 원하는 교수님이 2-3명 있는 대학원에 지원을 하던가 대학원 네임벨류만 보고 이 대학원 박사면 다 좋으니 일단 들어가서 어느 교수님이든 함께 연구해보겠다 하는겁니다. 네임벨류만 보겠다면야 하버드, 엠아이티, 스탠포드 등 그냥 유명 대학원에 다 지원하는 식이고 특별한 연구 목표가 있는 경우면 유럽까지도 고려하실 수 있습니다.
Reply
장영우
3/5/2022 06:02:46 pm
헷갈려서 질문 드려봅니다.제가 알기로 nature 2019년 telomeres and telomerase:three decades of progress라는 논문에서 Watson이 'end replication problem' 을 주장하여 genome이 복제 될때 마다 telomere 길이가 줄어든다고 주장 하였는데 blackburn이것을 실험적으로 증명한건가요?
Reply
관리자
3/5/2022 06:50:16 pm
왓슨은 염색체 말단이 짧아 지는 문제를 지적한거고 그 말단에 특별한 서열이 존재함을 발견하여 텔로미어란 개념이 생긴게 블랙번 교수가 포닥시절에 일어난 일입니다. 이후 텔로미어의 흥미로운 기능들을 여러 실험을 통해 알아내었고 결국 텔로미어제라는 텔로미어를 늘리는 효소를 찾아내며 노벨상을 탄거에요. 그 당시는 텔로미어 수축이 수명을 제한한다 믿었으니 이를 늘리는 텔로미어제의 발견은 엄청난 가능성을 암시했거든요.
Reply
장영우
4/9/2022 11:42:11 pm
링크로 올려주신 Inhibition of 'jumping genes' promotes healthy ageing의 논문의 figure1에서
관리자
4/13/2022 09:35:31 am
네이처 논문의 데이터를 기반으로 모델을 제시한거고 네이처 논문의 막대 그래프들이 early 와 late SASP 의 차이를 보여줍니다. figure caption 에 나왔듯 요약하자면: In Leave a Reply. |




 RSS Feed
RSS Feed
