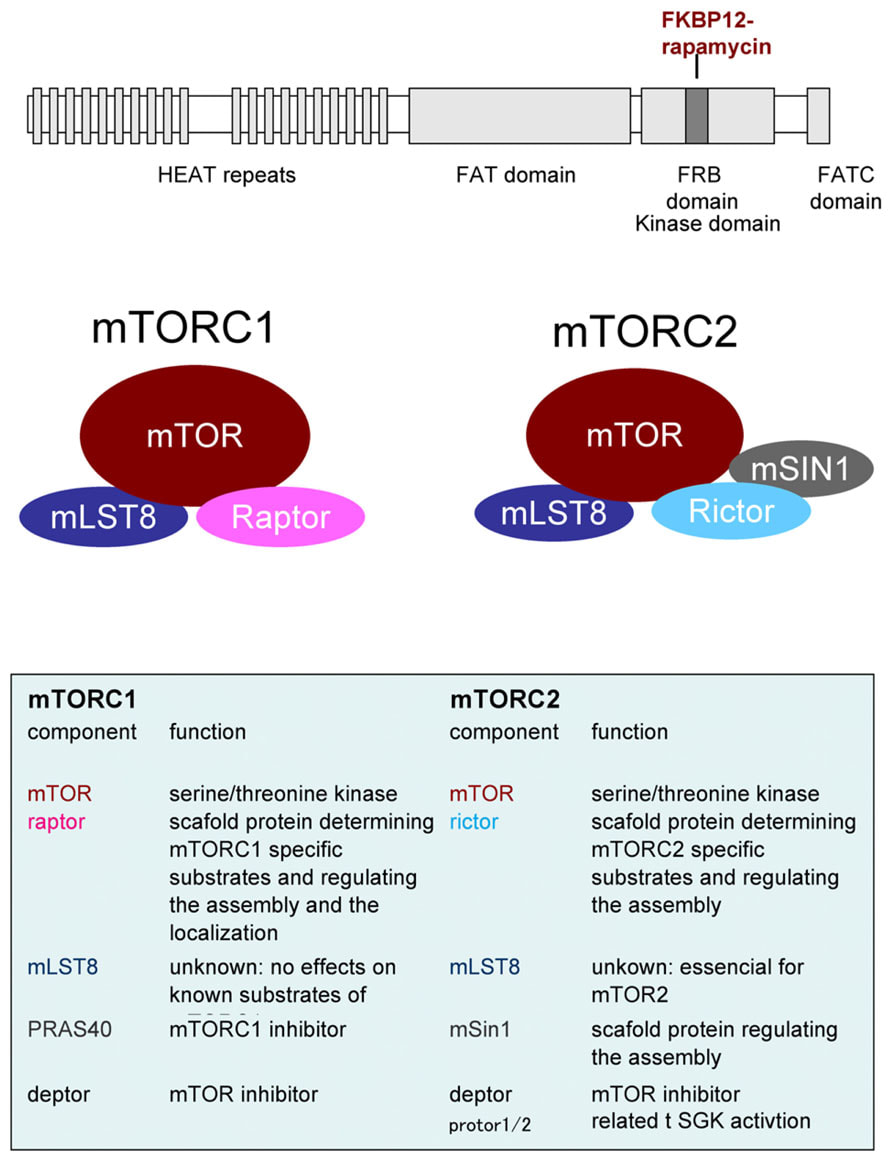
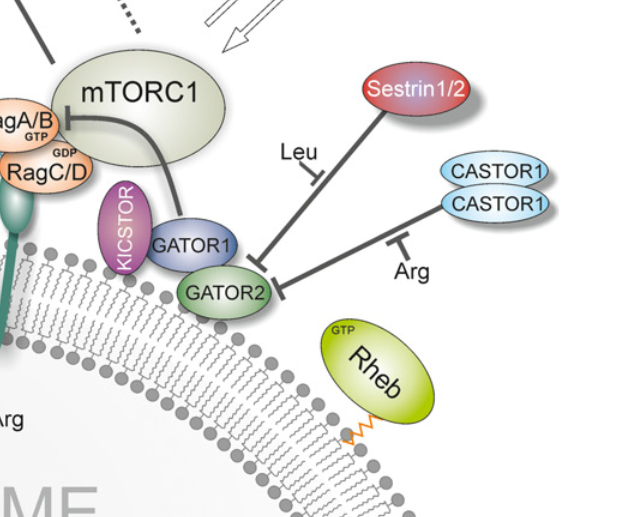
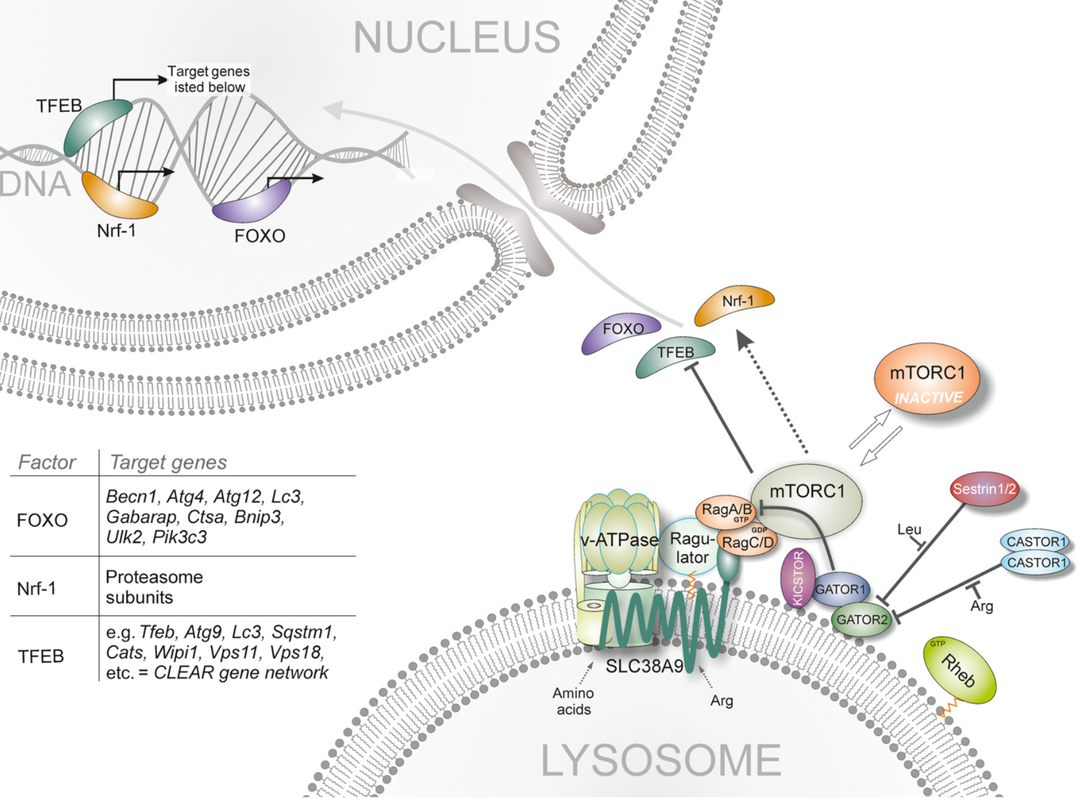
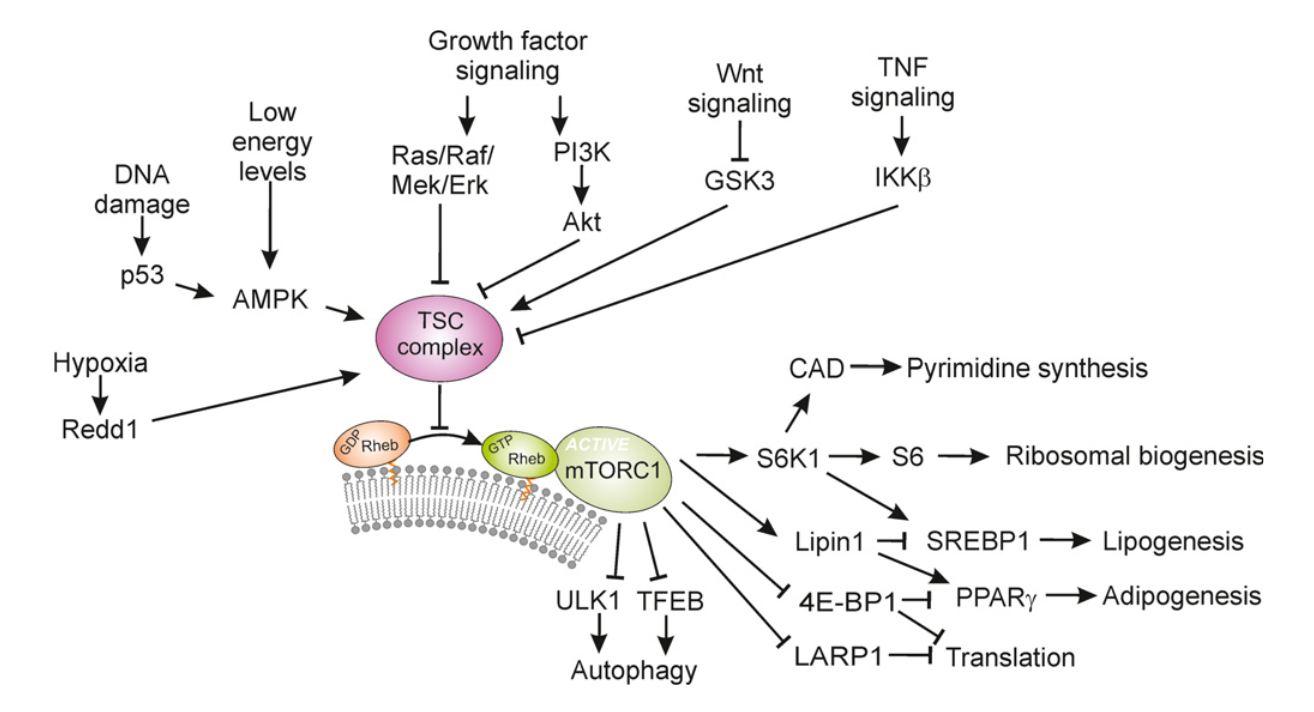
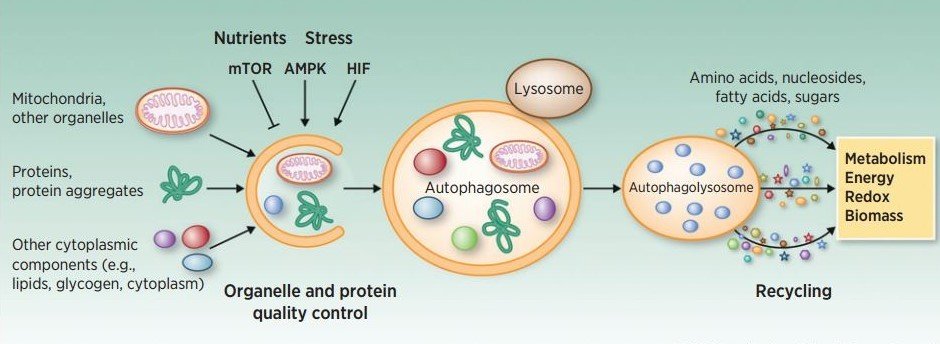
mTOR과 자가포식의 관계TOR-mediated regulation of metabolism in aging Antikainen et al. 2017 노화의 원인을 찾기 위한 노력 끝에 몇 가지 대표적인 이론들이 탄생했다. 그중 하나가 브레이크 없는 mTOR로 인한 노화다. mTOR은 포유류(mammalian)의 TOR이란 뜻이고 여기서 TOR은 target of rapamycin, 즉 라파마이신의 타겟이란 뜻이다. 건강에 관심이 많은 사람이라면 라파마이신이 뭔지 알 거다. 노화를 막을 수 있다고 광고 되는 기적의 신약이다. 문제는 정말 노화를 막는지 보려면 수십 년 동안 복용을 해봐야 안다는 것이고 장기 복용 시 부작용이 일어나진 않을지 우려도 있다. 라파마이신을 발견해 회사를 차린 교수님은 지금 호화롭게 살고 계시지만 동료 교수님들은 불완전한 과학을 팔아 돈을 벌고 있다며 비난을 하기도 한다. 그럼 mTOR이 뭐길래 mTOR을 막으면 노화가 멈춘다 주장하는 것일까? mTOR은 발달과 성장에 핵심적인 유전자다. 거의 모든 생물은 태어나서 얼마 안 있어 성장기를 거친다. 이때 폭발적인 성장을 가능케 하는 게 mTOR이고 마치 슈퍼카의 고성능 엔진과 같이 큰 힘을 발휘하여 모든 세포가 빠르게 성장하고 분열하게 만든다. 문제는 성장기가 지나도 mTOR이 멈추지 않는다는 것이다. 이미 필요한 세포를 다 만들었고 더 이상 성장할 자리도 없는데 한번 시작된 고성능 엔진은 꺼질 생각을 안한다. 슈퍼카를 가지고 레이싱 트랙을 원 없이 달릴 땐 기분이 좋았는데 트랙을 나와서 좁은 골목길을 천천히 가려니까 잘 조절되지 않아 여기저기 사고를 일으키고 만다. 이게 바로 mTOR 중심 노화 이론이다. 성장기 때 큰 공을 세운 mTOR이 브레이크 없는 자동차처럼 계속 불필요한 성장을 유도하니까 몸이 견디지 못해 조금씩 상하게 된다는 생각이다. 이번 리뷰에선 이 유명한 mTOR과 자가포식이라는 비교적 새로운 노화 이론의 관계성을 설명한다. 리뷰를 읽기 시작하고 얼마 안 돼서 급 후회하였다 [출처]. 생물학에서 가장 복잡한 주제인 신호 전달 경로가 대거 등장한다. 그만큼 mTOR이 중요한 역할을 갖고 있다는 뜻이기도 하지만 도저히 설명할 자신이 없다. 등장하는 경로 하나하나를 풀이하자면 포스팅 수십 개는 해야 할 거 같고 그렇게 장황한 내용은 지루해서 아무도 안 읽을 거다. 일단 선정을 했으니 간략하게나마 소개를 하겠지만 mTOR에 대한 자세한 리뷰는 훗날 다시 하겠다. 그때쯤이면 여러 경로에 대한 리뷰들이 많이 축적됐을 거니 장황한 설명을 참고 링크로 대체하겠다. mTOR은 앞서 말했듯 mammalian target of rapamycin의 약자다 [출처]. 라파마이신이란 노화를 저지하는 기적의 약이 먼저 발견됐고 이 약의 원리를 연구하다 보니 mTOR이라는 단백질 복합물이 핵심적임을 알아냈다. 참고로 mTOR 은 엠-톨 이라고 읽는다. mTOR 복합물은 두 가지가 있다. mTORC1과 mTORC2라 부르는데 대부분의 mTOR 연구는 mTORC1에 대한 것이고 mTORC2에 대한 연구는 아직 부실한 편이다. mTOR을 저지하면 수명이 늘어나고 노화가 늦춰진다. 이는 mTOR 억제제인 라파마이신을 복용한 예쁜꼬마선충, 초파리, 그리고 가장 최근엔 애완견을 통하여 입증된 바다 (애완견을 이용한 연구는 모순된 결과가 좀 있었지만..). mTOR 신호 전달 경로도 꽤 자세히 밝혀졌는데 먼저 Sestrin이라는 스트레스 감지 단백질에서 시작된다. Sestrin은 p53, FOXO, pCREB 등의 신호를 받아 GATOR이라는 단백질에 영향을 행사한다. 이 과정에서 루씬과 아르기닌이라는 아미노산의 존재 여부에 따라 GATOR이 억제될지 말지 결정된다. GATOR은 Rag라는 단백질을 억제하는데 Rag는 mTORC1을 리소좀에 붙여 활성화하는 밧줄 같은 거다. 글보다는 그림이 훨씬 이해가 편한 부분이다. 이렇게 mTORC1이 리소좀에 장착되면 그다음엔 Rheb이라는 게 mTORC1의 스위치 역할을 한다. Rheb 또한 여러 신호에 반응하는데.. 정말 많은 신호에 반응한다.. PI3k, Ras, Akt/PKB, Erk1,2, IGF1, Wnt, TNF-a ... 생화학을 이수했다면 어렴풋이나마 뭔지 알거지만 전문가가 아니면 뭐가 뭔지 모르는 게 당연하다. 그냥 다양한, 아주 중요한 신호 전달 경로가 다 mTOR로 이어진다고 알면 된다. (Wnt 신호 전달 경로에 대해선 노화 유전자 SITRUIN 이란 포스팅을 참고해도 좋다) 어쨌건 다양한 신호에 반응하여 mTOR 이 활성화 되면 세포 성장을 유도하는 전사 인자들을 핵으로 들여보네 세포 성장을 이끄는 거다. 중요한 건 mTOR의 활성화 과정중에 양분 감지 단계가 들어있다는 거다. 소식하면 장수하고 열량을 제한시키면 노화가 늦어짐은 이미 알려져 있었다. 이제 보니 열량 제한은 mTOR을 억제해 노화를 늦춘걸로 보인다. 같은 맥락에서 특정 아미노산만 제한해도 같은 효과 혹은 더 좋은 효과를 보인 사례가 있고 반대로 어릴 때 과도한 당분 섭취가 수명을 단축한 연구 결과도 있다. mTOR이 수명을 결정하는데 매우 중요한 녀석인데 왜 세포핵도 아닌 리소좀에 붙어 있는 걸까? 아니 꼭 어디 붙어야 중요한 일을 하는 건 아니지만 라이소자임이란 소기관은 좀 뜬금없는 위치 같다. 리소좀은 소화 효소가 잔뜩 들어있는 슬라임 같은 거다. 불필요한 단백질이나 소기관을 흡입하여 분해하는 일을 한다. 수명을 결정하는데 핵심적인 mTOR이 리소좀에 붙어 있는 게 단순한 우연일까? 아니면 세포속 청소부 리소좀이 우리가 모르는 중요한 일을 하고 있는 걸까? 이런 생각에서 비롯된 게 자가파괴와 노화의 연관성 연구다 [출처]. 자가파괴는 앞서 설명한 리소좀의 청소부 일을 고급지게 표현한 단어다. 단순히 불필요한 것을 분해하여 양분을 재활용하는 것이면 양분이 넉넉한 지금 우리에겐 그리 중요한 일이 아닐 것이다. 하지만 자가파괴는 고장 난 단백질이 세포 안에서 문제를 일으키지 않도록 바로 제거하며 정확히 필요한 양의 단백질이 유지될 수 있도록 조율하는 단백질 품질 검사와 마이크로 컨트롤을 하고 있다.
꼬마선충의 자가파괴에 필수적인 유전자 age-1과 daf-2가 변이될 경우 라파마이신으로 mTOR을 억제해도 수명 연장 효과를 볼 수 없었고 다른 생물에서도 자가파괴 필수 유전자가 제거될 경우 mTOR 억제로 인한 효과가 사라졌다. 다시 말해 노화를 늦추고 수명을 연장하기 위해 필요한 조건은 mTOR의 억제와 원활한 자가파괴다. 흥미롭게도 이 둘 다 리소좀에서 일어나는 일이고 둘 다 양분 환경에 반응한다. 그동안 무시되던 리소좀을 조금 더 띄워주고 싶지만 리소좀으로 인한 자가파괴가 단백질 품질과 양을 정하는 유일한 방도는 아니다. 이전 리뷰에서 언급한 죽음의 마크 유비퀴틴만 생각해 보더라도 단백질 항상성이 중요한 만큼 조율하는 작용도 다양함을 알 수 있다. 이 정도면 mTOR에 대해 대충 설명이 될 듯 하니 리뷰 나머지 부분은 건들지 않겠다. 정리하자면 mTOR이 브레이크 없는 엔진으로 노화를 이끌어 왔다 알려졌는데 mTOR을 저지할 양분 감지와 자가파괴 능력에 관해 설명한 리뷰다. 아무리 브레이크 없는 엔진이라도 연료가 부족하면 느려지게 된다. mTOR이 과도하게 움직여 모두 폭삭 늙어버리는 일이 없도록 식탐을 줄이고 절제된 식습관을 갖자.
11 Comments
행인
3/23/2018 07:25:16 pm
좋은글입니다.
Reply
관리자
3/26/2018 04:50:40 am
대부분 아미노산은 어차피 몸에서 만들어 내기 때문에 섭취를 제한해도 별 효과가 없고 필수 아미노산이라 불리우는, 몸에서 만들어 낼 수 없는 것들을 제한해야 금식하는 효과가 나타납니다.
Reply
관리자
3/26/2018 04:53:26 am
그렇다고 필수 아미노산 섭취를 거부하거나 무작정 금식하면 안되요.. 섭취를 안하면 죽으니까 필수 아미노산이라 불리우는 겁니다. 몸의 노화를 늦추기 위해 소식하고 재생을 촉진시키기 위해 간헐적 단식을 하면 좋다는것이지 무조건 안먹으면 노화와 상관 없이 바로 죽습니다.
Reply
한정재
7/28/2018 08:15:17 am
저는 한줄기의 빛과 같은 이 싸이트를 발견하고 친구들에게 전파하고 있는 고3 학생입니다. 제 꿈은 노화라는 질병을 해결하는 것 입니다. 선생님(?)이 올려주신 글을 읽으며 꿈을 구체화 시키고는 있지만 어떤 대학을 어떤 학과를 진학해야할지를 모르겠습니다. 이런 생명공학(?) 관련 된 학과와 그런 학과가 유망한 대학을 추천해 주셨으면 합니다. 감사합니다.
Reply
관리자
7/28/2018 08:35:15 am
한줄기 빛이라니 부끄럽습니다.. 바뻐서 두달만 쉬어야지 한게 벌써 서너달이 되버렸네요. 한달만 더 쉬었다 오겠습니다.
Reply
관리자
7/28/2018 08:53:12 am
조금 현실적인 이야기를 하자면 박사는 미국에서 하셔야 합니다. 한국의 대학들도 점점 발전하고 있고 개인적으로 응원하는 마음과 함께 미래에 대한 기대가 큽니다. 하지만 이제 겨우 대학 연구가 조금씩 시작되고 있는 상태고 젊은 30대 교수님들 중 일부가 해외에서 공부해 온것으로 활발한 연구 활동을 시작하는 단계에요. 생물 연구는 특히 오랜 내공이 쌓여야 해서 50-60 대 교수님들이 분야를 이끄시는데 아직 한국엔 그런 분들이 흔치 않습니다.
Reply
관리자
7/28/2018 09:04:11 am
여건이 안돼 학부를 미국으로 가는건 불가능 하다면 한국내 최고 대학에 가서 그나마 연구를 활발히 하시는 교수님 랩에 들어가세요.
Reply
관리자
7/28/2018 09:22:04 am
두번째 글이 짤렸는데 그냥 미국 학부 연구와 한국 학부 연구는 전혀 다르다는 내용입이다. 한국 교수님들이 뭐가 부족하다는게 아니라 대학 설립 역사가 짧고 체계를 잡아가는 과정이다 보니 교수님들이 강의와 학교일에 치여 연구를 포기하실수 밖에 없고 차차 나아지겠지만 현재는 국제적으로 의미있는 대학 연구가 불가능한 상황입니다. 논문의 질과 사회적, 학문적 임팩트 보다 SCI 논문 숫자로 실적을 측정하는 것만 봐도 어떤 상황인지 알수 있죠.... 연구를 하시려면 해외로 나가셔야 해요.
Reply
abyTs
2/4/2019 10:57:25 pm
유튜브에서 맞춤 동영상으로 우연히 금식에 대해 알고, 호기심이 생겨 구글링하다 여기까지 온 19살 무직 사람인데요, 운동에 관심이 많아 엠톨이란 단어를 들어본 적이 있어요. 제가 들은 기억으로는 엠톨이 활성화가 되어야 근성장이 이뤄진다고 해서 그렇게 알고 있었는데 노화와 밀접한 관계가 있는줄은 몰랐네요. 여담이지만 저런 정보들을 보니 급 공부가땡기네요ㅎ;(고1 퇴학) 학교 다닐 때까지만 했어도 과학에 관심이 있었는데.. 윗댓 보면서 조금 더 열심히 살아야겠다고 생각했습니다.
Reply
aromatase
8/10/2021 01:38:52 pm
유익한 정보 감사합니다
Reply
ㅇㅇ
10/7/2021 08:41:51 pm
좋은 글 감사합니다!!!
Reply
Leave a Reply. |
Archives
August 2018
Categories |

 RSS Feed
RSS Feed
